Mitä ovat geneeriset lääkkeet?
Lääketieteelliset toimittajat tarkistavat kaiken -sisällön.Geneeriset lääkkeet (yksittäinen: geneeriset lääkkeet) ovat kopioita samasta vaikuttavasta aineesta (kopiovalmisteet) lääkkeistä, jotka ovat jo markkinoilla ja joiden patenttisuoja on päättynyt.

Uudet lääkkeet on patentoitu 20 vuoden ajan. Tänä aikana lääkeyhtiö voi myydä yksinomaan alkuperäistä valmistettaan ja määrittää sen hinnan. Valmistaja yrittää korvata uuden vaikuttavan aineen tutkimisesta ja kehittämisestä aiheutuvat korkeat kustannukset. Valmistajat kuitenkin yleensä hakevat patenttia uudelle vaikuttavalle aineelle sen ollessa vielä kehitteillä. Heti kun se tulee markkinoille, osa kahdenkymmenestä vuodesta on ohi.
Patenttisuojan päättymisen jälkeen alkuperäisen valmisteen valmistajan on julkaistava tutkimustulokset kyseisestä vaikuttavasta aineesta. Muut valmistajat voivat sitten käyttää näitä tietoja aktiivisen ainesosan tuottamiseen ja tuoda sen markkinoille geneerisenä tuotteena.
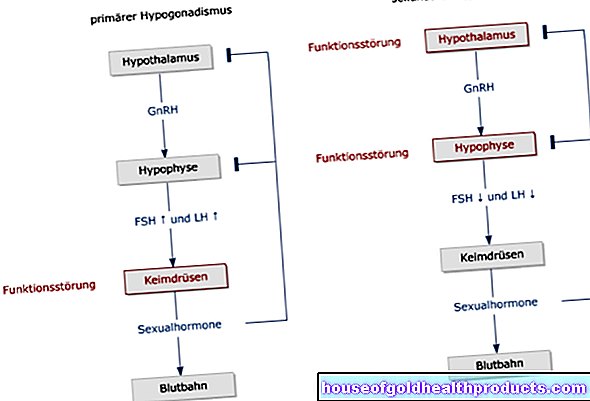
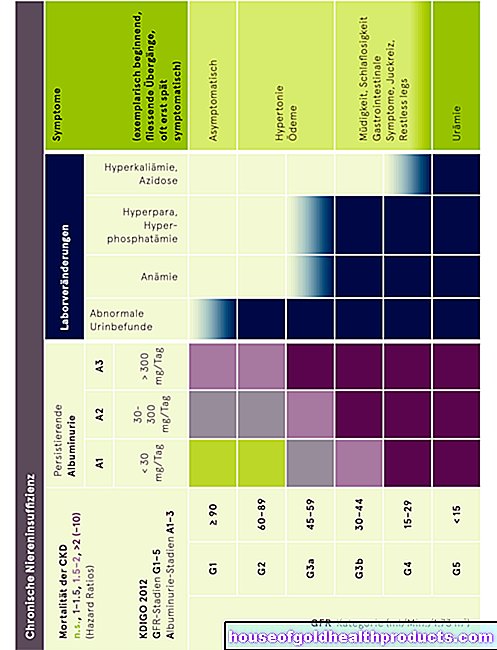
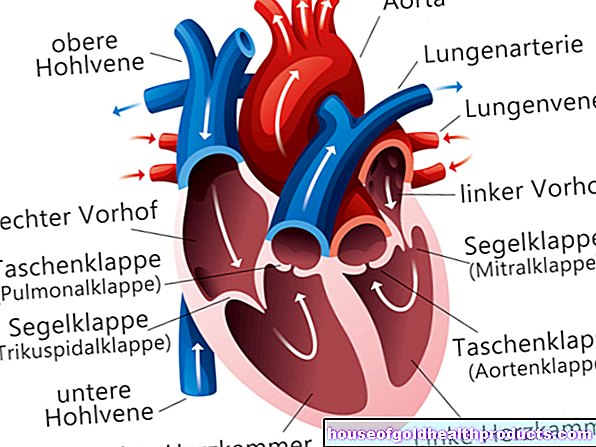
Nyt on yksi tai useampi geneerinen lääke lähes jokaiselle lääkkeelle, jonka patenttisuoja on päättynyt. Tämä koskee sekä käsikauppalääkkeitä, kuten kevyitä päänsärkyä lievittäviä lääkkeitä, että reseptilääkkeitä, kuten korkean verenpaineen, munuaisten vajaatoiminnan, diabeteksen tai jopa syövän valmisteita.
Terapeuttisesti vastaava
Geneeristen lääkkeiden valmistajien on osoitettava sääntelyviranomaisille, että geneerinen tuote vastaa laadultaan ja tehokkuudeltaan alkuperäistä. Tätä ei kuitenkaan tarvitse tehdä suurissa kliinisissä tutkimuksissa ja toksikologisissa tutkimuksissa, vaan ns. Bioekvivalenssitodistus riittää. Näin ollen geneeristä ja alkuperäistä pidetään bioekvivalenttina - toisin sanoen terapeuttisesti ekvivalenttina - jos ihmiskeho absorboi vaikuttavan aineen geneerisestä lääkkeestä suunnilleen samalla nopeudella ja suunnilleen samassa määrin kuin alkuperäinen (biologinen hyötyosuus).
Sana "suunnilleen" tekee jo selväksi, että lainsäätäjä sallii tietyn vaihteluvälin: se on 80-125 prosenttia. Esimerkiksi geneerisen aineen aktiivinen ainesosa voi imeytyä vain 90 prosenttiin tai 115 prosenttiin alkuperäisestä. Käytännössä useimpien kopiolääkkeiden poikkeama on kuitenkin vain noin viisi prosenttia.
Monissa tapauksissa tämä pieni poikkeama ei ole tärkeässä roolissa. Joillakin lääkkeillä se kuitenkin riippuu tarkasta vaikutuksen nopeudesta. Näissä tapauksissa viranomaiset voivat asettaa toleranssialueen lähemmäksi.
Bioekvivalenssin toleranssi on tarpeen, koska vaikuttavan aineen imeytymisnopeus ja -määrä voivat vaihdella hieman henkilöstä toiseen. Esimerkiksi sukupuoli ja ikä vaikuttavat tähän. Näin ollen yksittäisten bioekvivalenssitestin kohteiden mittaustulokset ovat usein erilaisia.
Sama annosmuoto
Geneeristen lääkkeiden on oltava samassa annosmuodossa kuin alkuperäinen. Kuitenkin esimerkiksi kaikkia suun kautta (eli suun kautta) otettuja valmisteita pidetään samoina. Tämä tarkoittaa: jos alkuperäinen on tabletti, geneerinen lääke voi tulla myyntiin myös kapselina tai rakeina.
Ero geneeristen ja alkuperäisten välillä
Geneerisen ja sen alkuperäisen valmisteen välillä voi olla eroja lisäaineissa (esim. Säilöntäaineet ja väriaineet) ja valmistusprosessissa. Lisäaineiden ja / tai valmistusprosessin kehittäminen voi parantaa kopiointituotetta jollakin tavalla. Tämän seurauksena sillä voi esimerkiksi olla pidempi säilyvyysaika, helpompi annostella tai joillekin ihmisille paremmin siedetty kuin alkuperäinen valmiste.
Lisäksi geneerisestä voi tulla alkuperäisen pitkävaikutteinen versio muokatun valmisteen kautta: Aktiivista ainesosaa ei sitten vapaudu nopeasti ja kerralla, kuten tässä tapauksessa, vaan hitaasti ja jatkuvasti. Tämä takaa aktiivisen ainesosan jatkuvan tason. Tällaisissa tapauksissa geneeriselle lääkkeelle, kuten alkuperäiselle, on kuitenkin tehtävä laaja kliininen tutkimus ihmisillä ennen kuin se voidaan hyväksyä.
Miksi geneeriset lääkkeet ovat halvempia kuin alkuperäiset?
Geneeriset palveluntarjoajat kehittävät kopiointituotteitaan alkuperäisen valmistajan tutkimustulosten perusteella. Periaatteessa tästä aiheutuvat vain valmisteen tai sen valmistuksen kustannukset (esim. Muut apuaineet). Alkuperäinen valmistaja on jo vastannut valtavista kustannuksista itse vaikuttavan aineen tutkimuksesta ja kehittämisestä.
Geneerisen lääkkeen hyväksyminen on myös paljon halvempaa: geneerisille lääkkeille määrätyt bioekvivalenssitestit ovat vähemmän aikaa vieviä ja paljon halvempia kuin alkuperäisen valmisteen kliiniset tutkimukset.
Kaiken kaikkiaan geneeristen toimittajien on investoitava tuotteeseensa paljon vähemmän rahaa kuin alkuperäisen valmisteen valmistaja. Voit siis tarjota sitä myös paljon halvemmalla.
Hinnoittelun kannalta myös toinen tekijä on ratkaiseva: Heti kun vaikuttavan aineen patenttisuoja on päättynyt, useat geneeristen lääkkeiden valmistajat yrittävät yleensä myydä kopioituja tuotteitaan samanaikaisesti. Ja kuten muillakin toimialoilla, sama pätee myös täällä: enemmän kilpailua - alhaisemmat hinnat.
Säästöjä terveydenhuoltojärjestelmässä
Kopioidut huumeet kattavat nyt 75 prosenttia lakisääteisten sairausvakuutuskassojen (GKV) huumevaatimuksista, mutta muodostavat alle kymmenen prosenttia lääkekuluista. Joten jos lääkärit määräävät halvempia geneerisiä lääkkeitä alkuperäisten valmisteiden sijaan, tämä tarkoittaa säästöjä sairausvakuutusyhtiöille ja helpotusta terveydenhuoltojärjestelmälle.
Siksi liittovaltion terveysministeriö on laatinut asetuksen, jolla edistetään geneeristen lääkkeiden määräämistä ja vähennetään siten lääkekustannuksia-niin sanottu lakisääteisten sairausvakuutusyhtiöiden "Aut-idem" -sääntö: Jos lääkäri ylittää "Aut-idem" "lääkemääräyksen laatikkoa ei tarkisteta, proviisorin on annettava potilaalle yksi kolmesta halvimmasta vaihtoehtoisesta valmisteesta määrätyn (alkuperäisen) lääkkeen sijaan. Tämän valmisteen on sisällettävä sama vaikuttava aine kuin määrätty lääke ja sen on oltava sama vahvuus ja pakkauskoko. Lisäksi sen on oltava hyväksytty samalle käyttöalueelle ja sillä on oltava sama tai vastaava annostusmuoto.
Lisäksi reseptilääkkeiden kiinteän hinnan sääntelyn tavoitteena on hillitä huumeiden menojen valtavaa kasvua. Joillekin vaikuttavien aineiden ryhmille (esim. Beetasalpaajat, kolesterolia alentavat statiinit) on vahvistettu enimmäismäärät, jotka lakisääteiset sairausvakuutusyhtiöt korvaavat. Jos lääkkeen hinta ylittää kiinteän summan, vakuutetun on itse vastattava lisäkustannuksista - lakisääteisen, yleensä 5–10 euron lisämaksun lisäksi.
Tämä lisämaksu jätetään kuitenkin usein maksamatta halvoista lääkkeistä (kuten geneerisistä lääkkeistä): Jos lääkkeen hinta on vähintään 30 prosenttia alle kiinteän summan, se on vapautettu lakisääteisestä lisämaksusta. Tällä asetuksella lainsäätäjä haluaa varmistaa, että potilaat pyytävät lääkäreitään määräämään erityisen edullisia lääkkeitä.
Toinen säästömahdollisuus syntyy kilpailuvaikutuksesta: jos useat geneeriset lääkkeet ja alkuperäinen valmiste kilpailevat keskenään, kokonaishinnat laskevat.
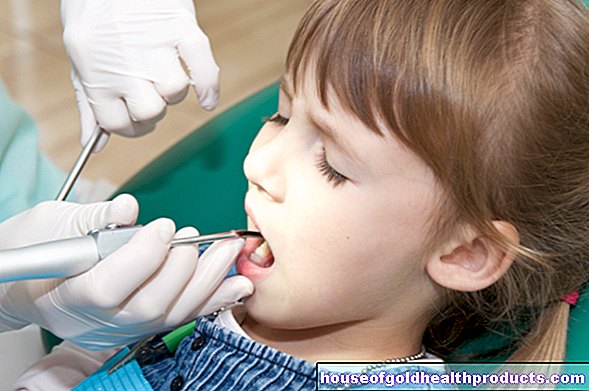
Yleislääkkeet lapsille
Toistaiseksi markkinoilla on vain muutamia lääkkeitä, jotka on erityisesti kehitetty ja hyväksytty lapsille. Siksi pienet käyttävät yleensä lääkkeitä, jotka on todella tarkoitettu aikuisille - sekä alkuperäisiä valmisteita että vastaavia geneerisiä lääkkeitä. Annosta pienennetään vastaavasti nuorille potilaille, jolloin lääkärin kokemus on ennen kaikkea tärkeä.
Mutta lapset eivät ole pieniä aikuisia - heidän kehonsa käsittelee huumeita usein eri tavalla kuin aikuisten. Tästä syystä EU antoi uuden asetuksen tammikuussa 2007: Sen jälkeen lääkkeiden valmistajien on täytynyt testata uusia (vielä hyväksymättömiä) valmisteita ja niitä, jotka ovat edelleen patenttisuojattuja alaikäisille, ja toimittaa tutkimustulokset hyväksyntäviranomaisille. Vastineeksi patenttisuojaa pidennetään molemmissa tapauksissa kuudella kuukaudella (vaikka alaikäisten testit olisivat negatiivisia eikä valmistetta ole hyväksytty lastenlääkkeeksi).
Muun muassa geneeriset lääkkeet on vapautettu tästä vaatimuksesta. EU on keksinyt heille jotain muuta: lääkeyhtiöt voivat myöhemmin mukauttaa aikuisille lapsille kehitettyä lääkettä (annoksena, annosmuodossa jne.). Euroopan hyväksyntäviranomaisen EMEA: n lastenlääkintäkomitea määrittelee oman testimenetelmänsä alaikäisille. Lastenlääke saa tällöin erityisen hyväksynnän, ns. PUMA (Pediatric Use Marketing Authorisation).
Lisäksi valmistaja "palkitaan" kymmenen vuoden asiakirjasuojalla: muut geneeristen lääkkeiden tarjoajat saavat tarkastella tutkimusasiakirjoja vasta tämän ajanjakson jälkeen, viitata siellä oleviin alaikäisiä koskeviin tutkimuksiin ja luoda lasten valmisteita uudelleen. Tämän vuoksi EU haluaa - eettisistä syistä - estää toista valmistajaa suorittamasta samoja testejä lapsilla tuodakseen markkinoille analogisen lasten geneerisen lääkkeen.