Selkärangan lihasten atrofia
ja Florian Tiefenböck, lääkäri PäivitettyMaximilian Reindl opiskeli kemiaa ja biokemiaa LMU: ssa Münchenissä ja on ollut -toimituksen jäsen joulukuusta 2020 lähtien. Hän perehtyy lääketieteellisiin, tieteellisiin ja terveyspolitiikan aiheisiin, jotta ne ovat ymmärrettäviä ja ymmärrettäviä.
Lisää viestejä käyttäjältä Maximilian ReindlFlorian Tiefenböck opiskeli ihmislääketiedettä LMU Münchenissä. Hän liittyiiin opiskelijana maaliskuussa 2014 ja on siitä lähtien tukenut toimitusta lääketieteellisillä artikkeleilla. Saatuaan lääketieteellisen lisenssin ja käytännön työn sisätautien hoidossa Augsburgin yliopistollisessa sairaalassa hän on ollut -tiimin pysyvä jäsen joulukuusta 2019 lähtien ja muun muassa varmistaa -työkalujen lääketieteellisen laadun.
Lisää viestejä käyttäjältä Florian Tiefenböck Lääketieteelliset toimittajat tarkistavat kaiken -sisällön.
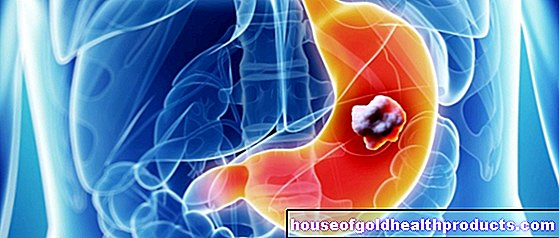
Selkärangan lihasatrofia tai lyhyesti SMA on harvinainen sairaus, jossa tietyt selkäytimen hermosolut kuolevat. Aivojen ärsykkeet ja impulssit eivät enää saavuta määränpäätä: lihaksia. Tämä aiheuttaa lihasten heikkenemistä ja halvaantumista. SMA: n muotoja on erilaisia. Vaikein alkaa lapsuudessa. Uudet hoidot lupaavat pysyvää terveyden paranemista. Lue lisää selkärangan lihasten atrofioista täältä.
Tämän taudin ICD -koodit: ICD -koodit ovat kansainvälisesti tunnustettuja koodeja lääketieteellisille diagnooseille. Ne löytyvät esimerkiksi lääkärin kirjeistä tai työkyvyttömyystodistuksista. G12

Lyhyt katsaus
- Mikä on selkärangan lihasten atrofia? Ryhmä lihasheikkoussairauksia. Ne perustuvat tiettyjen lihaksia (motorisia neuroneja) hallitsevien selkäytimen hermosolujen kuolemaan. Siksi SMA kuuluu motoristen neuronien sairauksiin.
- Mitä muotoja on olemassa? Perinnölliset selkärangan lihasatrofiat ovat enimmäkseen SMA: ta, jolla on tietty geneettinen vika kromosomissa 5 (5q-liittyvä SMA). Lääkärit erottavat neljä eri muotoa: SMA -tyyppi 1 - tyyppi 4. Lisäksi on satunnaisia muotoja, joiden perinnöllisyys ei ole varmaa.
- Esiintymistiheys: harvinainen sairaus; perinnöllinen SMA vaikuttaa noin yhteen vastasyntyneeseen 7000: sta.
- Oireet: lihasten nykiminen, etenevä lihasheikkous, lihasten heikkeneminen, halvaus. Liukuvärit vaihtelevat SMA -muodon mukaan.
- Syyt: Perinnöllinen selkärangan lihasatrofia 1-4 ovat seurausta kromosomin 5, tarkemmin sanottuna SMN1-geenin, geneettisestä viasta. Tämän seurauksena kehosta puuttuu erityinen proteiini, SMN -proteiini. Tämä vaje vahingoittaa selkäytimen motorisia neuroneja.
- Diagnoosi: Geneettinen tutkimus SMN: n geneettisen rakenteen muuttumisesta, fyysiset tutkimukset, elektroneurografia, elektromyografia, verikokeet (esim.
- Hoito: Geenikorvaushoito tai silmukointimodulaattoreiden lääkkeiden antaminen ovat mahdollisia. Mukana fysioterapia, puheterapia, kiputerapia ja psykoterapia. Tarvittaessa leikkaus selkärankaan. Hoitosuunnitelma SMA -tyypin mukaan.
- Ennuste: Perinnöllisen proksimaalisen SMA: n tapauksessa uusilla hoitovaihtoehdoilla on syy -vaikutus ja niillä voi olla positiivinen vaikutus taudin kulkuun. Hoidon aloittaminen aikaisin on ratkaisevan tärkeää. Hoidot eivät ole vielä kaikkien potilaiden saatavilla. Jos jätetään hoitamatta, SMA -tyypin 1 lapset kuolevat yleensä kahden ensimmäisen vuoden aikana. Tyypin 3 ja tyypin 4 elinajanodote tuskin tai ei lyhene.
Mikä on selkärangan lihasten atrofia?
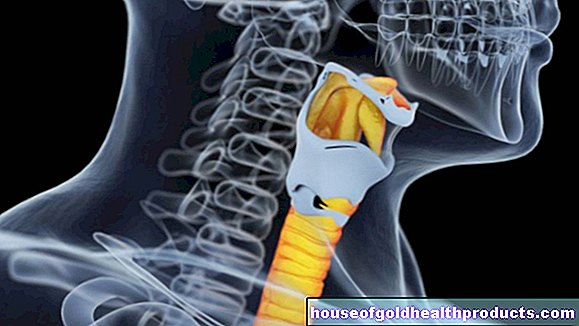
Selkärangan lihasatrofiassa (SMA) tietyt selkäytimen hermosolut kuolevat. Ne kontrolloivat yleensä lihaksia, minkä vuoksi asiantuntijat kutsuvat näitä hermosoluja motorisiin neuroneihin. Näin ollen SMA kuuluu ns. Motorisiin hermosairauksiin.
Selkärangan lihasten atrofioiden tapauksessa alemmat (toiset) motoriset neuronit, jotka ovat suoraan yhteydessä lihaksiin niiden lisäyksillä, vaikuttavat. Vaurion seurauksena vähemmän tai ei ollenkaan hermosignaaleja saavuttaa lihaksia. Lihakset heikentyvät ja pienenevät (lihasten tuhoutuminen / lihasten surkastuminen).
Lääkärit erottavat eri selkärangan lihasatrofian muodot. Ylivoimaisesti suurin ryhmä on perinnöllinen SMA, jossa rungon lähellä olevat (proksimaaliset) lihakset vaikuttavat. Ne perustuvat tiettyyn geneettiseen vikaan. Noin yksi seitsemästä vastasyntyneestä kehittää sen.
Selkärangan lihasatrofia on yleisesti harvinainen sairaus. Siitä huolimatta se on toiseksi yleisin autosomaalinen resessiivinen perinnöllinen sairaus, mutta myös yleisin vauvojen tai pikkulasten kuolinsyy geneettisen vian vuoksi.
Millaisia selkärangan lihasatrofioita on olemassa?
Lääkärit erottavat perinnölliset (perinnölliset) SMA -muodot satunnaisista muodoista. Toinen selkärangan lihasatrofian luokitus liittyy ensisijaisesti ensin vaikuttaviin lihasryhmiin. Siellä on
- Proksimaalinen SMA: Noin 90 prosentilla he muodostavat suurimman SMA -ryhmän. Oireet alkavat rungon lähellä olevista lihaksista eli proksimaalisesti.
- Ei-proksimaalinen SMA: Tässä vaikuttavat ensin kaukaiset lihasryhmät, kuten kädet ja jalat (distaalinen SMA). Jatkossa nämä SMA -levyt voivat levitä myös kehon keskellä oleviin lihaksiin.
- Erityiset muodot (esim.Kennedyn tyyppinen spinobulbar -lihasten atrofia)
Selkärangan proksimaaliset lihasten atrofiat
Perinnölliset proksimaaliset selkärangan lihasatrofiat ovat enimmäkseen sairauksia, jotka perustuvat tiettyyn geneettiseen vikaan (5q-liittyvä SMA, vika kromosomissa 5). Nämä puolestaan on jaettu neljään eri muotoon. Luokitus perustuu ensimmäisten oireiden ilmenemisaikaan ja taudin kulkuun.
Selkärangan lihasatrofia Tyyppi 1: Tämä on yleisin ja vakavin SMA -muoto. Sitä kutsutaan myös "Werdnig-Hoffmannin taudiksi" tai "akuutiksi infantiiliseksi SMA: ksi". Tauti alkaa yleensä varhaislapsuudessa. Lihasheikkous vaikuttaa koko kehoon - lääkärit puhuvat myös "levykkeen oireyhtymästä" (englanniksi floppy = flaccid, infant = infant, child). Useimmat hoitamattomat lapset, joilla on tyypin 1 SMA, kuolevat ennen kuin ovat kaksivuotiaita.
Selkärangan lihasatrofia, tyyppi 2: Tämä SMA -muoto tunnetaan myös nimellä "spinaalinen lihasten välinen atrofia" tai "krooninen infantiili SMA". Ensimmäiset oireet ilmenevät tyypillisesti ennen 18 kuukauden ikää. Potilailla on joskus merkittävästi lyhyempi elinajanodote.
Selkärangan lihasatrofia tyyppi 3: Se tunnetaan myös nimellä "nuorten selkärangan lihasatrofia" tai "Kugelberg-Welanderin tauti". Tämä SMA alkaa yleensä 18 kuukauden iän jälkeen ja ennen varhaista aikuisuutta. Lihasheikkous on lievempi kuin tyypissä 1 tai 2. Sairastuneilla on vain hieman lyhyempi elinajanodote.
Selkärangan lihasatrofia, tyyppi 4: Se on samanlainen kuin SMA -tyyppi 3, mutta se ilmenee vain aikuisena (yleensä> 30 vuotta). Lihasheikkous on kuitenkin vähemmän selvä ja etenee hitaammin kuin tyypin 3 SMA: lla.
Siirtymät eri versioiden välillä ovat sujuvia. Joissakin tapauksissa tämä vaikeuttaa selkeää rajaamista. Joillakin geneettisillä taipumuksilla on myös tärkeä rooli kyseessä olevan taudin vakavuudessa.
Muut selkärangan lihasatrofiat
Näiden proksimaalisten muotojen lisäksi on muitakin selkärangan lihasatrofian muotoja. Näitä ovat esimerkiksi harvinaisemmat, myös perinnölliset distaaliset selkärangan lihasatrofiat. Niiden kanssa oireet alkavat tyypillisesti lihasryhmissä, jotka ovat kauempana kehosta.
Perintöä ei taata satunnaisen SMA: n tapauksessa. Lisäksi perinnöllistä kertymistä ei voida määrittää. Kirjallisuudessa nämä sisältävät:
- Hirayama -tyyppi (nuorten distaalinen SMA, tauti noin 15 -vuotiaana, vaikuttaa käsivarsien lihaksiin, yleensä pysähtyy jopa ilman hoitoa ja voi jopa parantaa)
- Vulpian-Bernhard-tyyppi (myös "flail-arm" -oireyhtymä, joka alkaa olkahihnassa, yleensä 40-vuotiaana)
- Duchenne-Aran-tyyppi (vaikutti aluksi käden lihaksiin, leviää kohti vartalon runkoa, yleensä 30 vuoden iän jälkeen)
- Peroneaalinen tyyppi ("flail-jalka" -oireyhtymä, ensin säären lihaksissa)
- Progressiivinen bulbar -halvaus (puhe- ja nielemishäiriöt, vaikuttaa noin 20 prosenttiin potilaista, joilla on amyotrofinen lateraaliskleroosi)
Jotkut satunnaiset SMA -muodot ("heiluvarren - / - jalan" oireyhtymä, etenevä bulbarhalvaus) lasketaan amyotrofisen lateraaliskleroosin (ALS) variantteihin erikoispiireissä. Tämä artikkeli käsittelee pääasiassa perinnöllisiä proksimaalisia selkärangan lihasten atrofioita.
Spinobulbar -lihasten atrofia
Spinobulbar tai bulbospinaalinen lihasatrofia (Kennedyn tyyppi, Kennedyn oireyhtymä) on perinnöllinen sairaus. Se alkaa usein nuoresta aikuisikään. Tämä erityinen SMA-muoto periytyy X-linkitetyssä resessiivisessä muodossa ja vaikuttaa siksi vain miehiin (koska miehillä on vain yksi X-kromosomi, naisilla toinen, terve X-kromosomi on hallitseva ja korvaisi vian).
Lihasten heikkous kehon lähellä olevissa lihaksissa jaloissa ja käsivarsissa tai hartioissa sekä kielen ja kurkun lihaksissa on yleistä. Tämän seurauksena kärsivillä on esimerkiksi puhumis- ja nielemisvaikeuksia. He myös valittavat vapinaa, lihaskramppeja ja nykimistä. Sairastuneilla miehillä on myös usein kipeitä kiveksiä ja ne ovat steriilejä. Lisäksi rintarauhaset suurenevat (gynekomastia).
Spinobulbar -lihasten atrofia on yleensä hidasta. Elinajanodote on tuskin rajoitettu.
Mistä tunnistat selkärangan lihasten atrofian?
Tyypillisiä selkärangan lihasatrofiaa ovat etenevä lihasheikkous halvaantumiseen (paresis) asti ja lihasten nykiminen. Hermovaurion seurauksena lihakset eivät enää saa sähköisiä impulsseja, mikä saa ne kutistumaan ajan myötä (lihasten surkastuminen). Tarkat merkit ja valitukset riippuvat lomakkeesta. Seuraavassa osassa tarkastellaan perinnöllisen proksimaalisen SMA: n oireita.
Infantiilisen selkärangan lihasatrofian tyypin 1 oireet
Tyypin 1 SMA: n oireet ilmenevät kuuden ensimmäisen elinkuukauden aikana. Yleistynyt lihasheikkous ilmenee - eli sellainen, joka vaikuttaa koko kehoon. Lisäksi lihasten välinen jännitys vähenee. Lääkärit puhuvat hypotoniasta.
Vastasyntyneillä tämä lihasheikkous ilmenee aluksi tyypillisessä jalan asennossa, joka muistuttaa makaavaa sammakkoa (sammakkojalkojen asento). Jalat ovat taipuneet, polvet ulospäin ja jalat sisäänpäin. Jopa pään nostaminen tai pitäminen yksin ei yleensä ole mahdollista.
Ikääntyneillä lapsilla, joilla on tyypin 1 SMA, ei voi istua tai kävellä yksin. Monet lapset eivät myöskään voi puhua, koska myös kielen lihakset voivat vaikuttaa.
Toinen tyypin 1 selkärangan lihasatrofian ominaispiirre on ylävartalon muoto: rinnan ja selän lihakset eivät kehity kunnolla. Tämä antaa ylävartalolle kellomaisen muodon (kellon rintakehä). Koska rintakehän ja selän lihakset ovat kehittyneet heikosti, kärsineet ottavat kumaran asennon.
Usein myös selkärangan kaarevuus (skolioosi) kasvaa. Kumartunut eteenpäin ja kumara asento aiheuttaa lisää hengitysvaikeuksia. Hyvin nopea ja pinnallinen hengitys (takypnea) on ominaista.
Oireet tyypin 2 selkärangan lihasatrofiasta
Tyypin 2 selkärangan lihasten atrofia aiheuttaa yleensä vain oireita 7–18 kuukauden iässä. Lapset voivat istua yksin, mutta eivät yleensä opi seisomaan tai kävelemään. Lihasheikkous etenee hitaammin kuin tyypissä 1.
Tyypin 2 SMA: lla samanlaisia oireita esiintyy vakavan lapsen muodon kanssa, kuten selkärangan muodonmuutos. Nivelet jäykistyvät lihasten ja jänteiden (supistumisten) lyhenemisen vuoksi. Muita merkkejä ovat käsien vapina ja kielen lihasten nykiminen.
Nuorten selkärangan lihasatrofian oireet, tyyppi 3
Tyypin 3 selkärangan lihasatrofia ilmenee tyypillisesti 18 kuukauden iän jälkeen ja ennen 18 vuoden ikää. Lapset voivat istua, seistä ja kävellä itsenäisesti. Lihasten heikkous, etenkin lantion ja jalkojen lihaksissa, aiheuttaa kuitenkin heilumista.
Suorituskyky heikkenee useiden vuosien aikana: Aluksi vammautuneiden mielestä urheilutoiminta tai portaiden kiipeäminen on vaikeaa, mutta lopulta on myös vaikea kantaa esimerkiksi ostoskasseja. Useiden vuosien jälkeen tyypin 3 selkärangan lihasatrofia tekee juoksemisesta ja muusta rasituksesta vaikeaa tai jopa mahdotonta jopa vanhuksilla.
Kaiken kaikkiaan oireet ovat kuitenkin vähemmän voimakkaita kuin kahdessa muussa sairaustyypissä, tyypissä 1 ja tyypissä 2. Monien sairastuneiden elämänlaatu ei heikkene pitkään aikaan.
Oireet aikuisen selkärangan lihasatrofiasta, tyyppi 4
Tämä hyvin harvinainen progressiivisen lihasten tuhoutumisen muoto alkaa aikuisikään, usein elämän kolmannelta vuosikymmeneltä. Jalkojen ja lonkan lihakset vaikuttavat aluksi. Taudin edetessä lihasheikkous leviää myös hartioihin ja käsivarsiin.
Kliinisen kuvan ilmenemismuodot ovat samanlaiset kuin nuorten SMA -tyypin 3 oireet. Kuitenkin progressiivinen lihasheikkous on jopa hitaampaa kuin tyypin 3 SMA: lla.
Mikä aiheuttaa selkärangan lihasten atrofian?
Selkärangan lihasatrofiassa toinen selkäytimen motorinen neuroni kuolee. Nämä ovat hermosoluja, jotka ohjaavat lihaksia liitteineen. Näiden erittäin erikoistuneiden motoristen neuronien vaurioiden seurauksena lihaksiin pääsee vähemmän sähköisiä signaaleja kuin terveillä ihmisillä. Jos lihassoluja käytetään vähemmän ja siksi vähemmän stimuloituina, keho hajottaa ne ajan myötä.
Geneettinen vika
Useimmissa tapauksissa selkärangan lihasatrofia on perinnöllinen sairaus (perinnöllinen SMA). Tyypillisten proksimaalisten SMA-muotojen syy on virheelliset tiedot potilaan geneettisestä rakenteesta. Kromosomissa 5 oleva niin kutsuttu SMN1-geeni ei ole toimiva.
SMN1 -geeni kuljettaa tietoa - eli suunnitelmaa - elintärkeästä SMN -proteiinimolekyylistä. SMN tarkoittaa "Survival (of) Motor Neuron". Ilman SMN -proteiinimolekyyliä motoriset neuronit tuhoutuvat ajan myötä.
On totta, että kehossa on myös siihen liittyvä SMN2-geeni, joka periaatteessa kykenee "kompensoimaan" ei-toiminnallisen SMN1-geneettisen informaation. Mutta tämä tapahtuu yleensä vain pienessä määrin. Tämä tarkoittaa sitä, että ehjää SMN2 -geenikopiota ei yleensä voida täysin korvata SMN1 -geenin toiminnan menetyksellä (jos sitä ei käsitellä).
Autosomaalinen resessiivinen ja autosomaalinen hallitseva perintö
Henkilön geneettiset tiedot ovat saatavilla kahtena kappaleena. Tämän seurauksena jokaisella on kaksi kopiota SMN1 -geenistä - yksi isältään ja toinen äidiltään. Lapsuuden proksimaaliset selkärangan lihasatrofiat periytyvät tyypillisesti autosomaalisena resessiivisenä piirteenä.
Tämä tarkoittaa, että molempien vanhempien geenivarianttien (alleelit) on oltava viallisia, jotta selkärangan lihasatrofia kehittyy jälkeläisissä. Resessiivisen perinnön tapauksessa vanhemmat eivät vaikuta, koska heillä on toimimattoman geenin lisäksi myös terve SMN1 -geeni, joka kompensoi vian.
Noin joka 45. henkilö on tämän SMA -järjestelmän omistaja. Pariskunnalla, jossa molemmat kumppanit ovat kantajia, on 25% riski saada lapsi, jolla on tauti.
Joissakin tapauksissa nuoruusiässä erityisesti selkärangan lihasten atrofiat aikuisuudessa seuraavat myös autosomaalista hallitsevaa perintöä. Jos kyseessä on hallitseva perintö, viallinen geeni väittää jo itsensä - ja kärsineet sairastuvat. Tämä ei kuitenkaan ole edellä mainittu geneettinen vika kromosomissa 5. Nämä 5q: hen liittyvät SMA: t periytyvät aina autosomaalisesti resessiivisellä tavalla.
Perintö muiden SMA -muotojen kanssa
Ei-proksimaalinen selkärangan lihasatrofia voi myös olla perinnöllinen. Erityinen spinobulbar -muoto (Kennedyn tyyppi) periytyy recessiivisesti sukupuolikromosomin, X -kromosomin, kautta (tämä vaikuttaa geenimuunnelmiin, jotka sisältävät suunnitelman miespuolisten sukupuolihormonien telakointialueille). Satunnaisten muotojen tapauksessa perintöä ei kuitenkaan taata. Täällä tiedetään vähän, miksi juuri toiset motoriset neuronit tuhoutuvat.
Tutkimukset ja diagnoosi
Selkärangan lihasatrofian diagnosoivat yleensä lastenlääkärit, hermosairauksiin erikoistuneet lastenlääkärit (neuropediatria) ja hermostosairauksien asiantuntijat (neurologit). Erilaiset tutkimukset ovat tarpeen tarkemman selityksen saamiseksi. SMA: n tapauksessa hermojen ja lihasten geneettiset testit ja tutkimukset ovat erityisen tärkeitä.
Kokoelma sairaushistoriaa (anamneesi)
Jokaisen sairauden yhteydessä lääkäri kysyy ensin oireista ja siitä, miten se on edennyt tähän mennessä. Vauvoilla ja pikkulapsilla vanhemmat ilmoittavat muutoksista ja poikkeavuuksista lapsensa käyttäytymisessä. Erityisesti perinnöllisten sairauksien osalta lääkärit keskittyvät myös perheen sairaushistoriaan.
Fyysiset tutkimukset
Periaatteessa lääkäri määrittää motorisen kehityksen poikkeavuudet tutkimalla lasta fyysisesti. Se esimerkiksi testaa, voivatko lapset itsenäisesti pitää päätään pystyssä, istua tai liikuttaa käsiään tai jalkojaan itsenäisesti (iästä riippuen).
Täydentäviä liikuntatestejä tehdään vanhemmille lapsille ja aikuisille, joilla epäillään selkärangan lihasten atrofiaa. Lääkäri tarkistaa, kuinka paljon henkilö voi kerätä voimaa ja kuinka kauan hän voi pitää sitä. Hän tutkii myös kestävyyttä.
Lisäksi lääkäri testaa refleksejä, jotka tyypillisesti heikkenevät tai sammuvat, etenkin selvien selkärangan lihasatrofioiden tapauksessa. Tätä varten hän napauttaa erilaisia jänteitä vasaralla, esimerkiksi kantapäähän tai polven alle, ja tarkistaa reaktion.
Geneettiset tutkimukset
Luotettavin (perinnöllisen) selkärangan lihasatrofian havaitsemismenetelmä on geneettinen analyysi.Lääkärit etsivät todisteita muuttuneesta (mutatoituneesta) SMN1 -geenistä ja olemassa olevien SMN2 -kopioiden määrästä.
Yleinen sääntö on diagnosoida ja hoitaa (perinnöllinen) SMA mahdollisimman varhaisessa vaiheessa. Muodosta ja käytettävissä olevasta hoidosta riippuen moottorin kehitykseen voidaan vaikuttaa positiivisesti ennen kuin selkäytimen motoriset neuronit vaurioituvat peruuttamattomasti.
Lisätutkimuksia SMA: ssa
Jos epäillään SMA: ta, lääkärit mittaavat usein hermojen johtumisnopeutta (elektroneurografia) ja lihasten toimintaa (elektromyografia). Tarvittaessa he tutkivat myös lihaksia ultraäänellä (myosonografia) tai magneettikuvauksella (MRI).
Lisäksi lääkärit järjestävät verikokeita. Jos selkärangan lihasatrofia esiintyy, tiettyjä parametreja voidaan muuttaa: esimerkiksi kreatiinikinaasipitoisuus (CK, tyypillinen lihasentsyymi) nousee.
Selkärangan lihasatrofioiden hoito
Selkärangan lihasatrofian hoito on monimutkaista. Kausaaliterapia ei ollut pitkään mahdollista minkään SMA: n muodon kannalta. Kuitenkin lääketieteellisen tutkimuksen edistyminen tarjoaa lääkäreille uusia hoitovaihtoehtoja auttamaan perusteellisesti niitä, joilla on proksimaalinen SMA (SMN -geenivika kromosomissa 5).
Lisäksi lääkärit keskittyvät oireiden lievittämiseen ja parhaan mahdollisen tuen antamiseen potilaille (esim. Fysioterapia, hengityshoito, psykoterapia, mahdollisesti leikkaus).
Lääketieteellinen hoito
Uudet hoitomenetelmät potilaille, joilla SMA perustuu tunnettuun SMN -geenivirheeseen, vaikuttavat suoraan itse geneettiseen materiaaliin tai geneettisen tiedon jatkokäsittelyyn.
Tavoitteena on, että potilaan keho pystyy itsenäisesti tuottamaan riittävästi SMN -proteiinia, joka on ratkaisevan tärkeää motorisille neuroneille.
Seuraavat hoitovaihtoehdot ovat käytettävissä selkärangan lihasatrofiaa varten:
- Silmukointimodulaattorit (Nusinersen, Risdiplam): Nämä lääkkeet puuttuvat suoraan lähetti -RNA -molekyylien jatkokäsittelyyn. Ne vahvistavat niitä prosesseja, jotka tuottavat suuremman määrän SMN -proteiinia koskemattomasta SMN2 -geenistä.
- Geenikorvaushoito (Onasemnogene Abeparvovec): Tämä hoito vaikuttaa suoraan ihmisen genomiin. Viallinen SMN1 -geenin kopio korvataan vaurioituneissa soluissa ulkoisesti toimitetulla, toiminnallisella geenikonstruktilla.
Jatkosmodulaattorit
SMN1 -geenivirheen tapauksessa keho voi vaihtoehtoisesti tuottaa SMN -proteiinin vastaavasta SMN2 -geenistä. Korvaava geeni SMN2 "hyppää sisään", mutta se ei riitä. Syy: SMN2: n proteiinit ovat yleensä liian lyhyitä ja hajoavat nopeasti.
Tämä johtuu vastaavan SMN2 -lähetti -RNA: n (SMN2 mRNA) käsittelystä. Se välittää rakentamistiedot genomista (DNA) proteiinin tuotantopaikoille (ribosomit).
Tätä varten ensin luetaan genomin SMN2 -geeni. Alustava SMN2 -lähetin -RNA tuotetaan. Sitä on muun muassa käsiteltävä edelleen ns. Silmukoinnin avulla. Vasta sitten syntyy kypsä lähetin -RNA. Erityiset solukompleksit, ribosomit, lukevat sitten kypsän lähetti -RNA: n ja tuottavat siten SMN2 -proteiinia. Ja juuri tämä on lyhennetty ja epävakaa, puretaan nopeasti eikä voi ottaa SMN1 -toimintoa haltuunsa.
Tämän muuttamiseksi vaikuttavat aineosat Nusinersen ja Risdiplam vaikuttavat alustavan lähetti -RNA: n jatkokäsittelyyn. Tämän seurauksena nämä niin kutsutut silmukointimodulaattorit lisäävät lopulta käyttökelpoisten SMN -proteiinien määrää - ja voivat siten varmistaa riittävän saannin.
Nusinersen
Lääke Nusinersen on niin kutsuttu "antisense-oligonukleotidi" (ASO). Euroopan lääkevirasto hyväksyi sen vuonna 2017. ASO ovat keinotekoisesti tuotettuja ja erityisesti mukautettuja RNA -molekyylejä. Ne sitoutuvat spesifisesti ja tarkasti SMN2 -lähetin -RNA: han. Tämä estää niitä käsittelemästä edelleen väärin ihmissolussa.
Erityisesti: Nusinersen estää tärkeiden tietojen (eksoni 7) leikkaamisen virheellisesti SMN2 -lähetti -RNA: sta. Eksonin 7 olinpaikka saa kehon tuottamaan myöhemmin toimivampaa SMN -proteiinia.
Nusinersen annetaan lannerangan kautta. Tämä tarkoittaa, että lääke ruiskutetaan selkäydinkanavaan ruiskulla. Tämä hoito toistetaan säännöllisin väliajoin muutaman kuukauden välein. Ensimmäisenä hoitovuonna sairastuneet saavat kuusi, sitten kolme annosta vuodessa.
Potilaat yleensä sietävät lääkettä hyvin. Nusinersen johtaa suotuisampaan tautikurssiin. Tutkimukset ovat osoittaneet, että liikkuvuus paranee monilla potilailla: monissa tapauksissa oli mahdollista istua vapaasti ja kääntää kehoa itsenäisesti. Haittavaikutukset ja komplikaatiot perustuvat muun muassa lannerangan puhkeamiseen (esim. Päänsärky, aivokalvon tulehdukset).
Risdiplam
Euroopan komissio hyväksyi Risdiplamin kolmanneksi lääkkeeksi 5q: hen liittyvää SMA: ta vastaan (tyypit 1-3 tai 1-4 SMN2-geenikopiota) maaliskuussa 2021. Risdiplam otetaan päivittäin liuenneena jauheena. Tarkka annos lasketaan iän ja ruumiinpainon perusteella.
Toisin kuin Nusinersen, Risdiplam ei ole "antisense -oligonukleotidi", vaan pieni molekyyli. Tämä molekyyli sitoutuu SMN2 -proteiinien lähetti -RNA: han ja vakauttaa ne tällä tavalla. Tämän seurauksena syntyy toimivampia SMN -proteiineja.
Risdiplamin yleisiä sivuvaikutuksia ovat ruoansulatuskanavan epämukavuus, ihottuma, kuume ja virtsatietulehdukset.
Geenikorvaushoito
Toinen lähestymistapa proksimaalisen selkärangan lihasatrofian hoitoon perustuu geenikorvaushoitoon. Viallinen SMN1 -geeni - progressiivisen SMA: n lähtökohta - "korvataan" uudella geenin toiminnallisella kopiolla.
Tällä periaatteella toimiva vaikuttava aine Onasemnogene Abeparvovec (AVXS-101) sai Euroopan lääkevirastolta (EMA) ehdollisen myyntiluvan pikkulasten ja lasten hoitoon toukokuussa 2020.
Lääkettä voidaan käyttää SMA -tyypin 1 hoitoon EMA -tietojen mukaan. Kaikissa muissa SMA -taudin muodoissa geneettiset ominaisuudet (SMN2 -kopioiden määrä) päättävät, onko geenikorvaushoito vaihtoehto.
Onasemnogene Abeparvovecin avulla toiminnallinen kopio ihmisen SMN1 -geenistä viedään selkäytimen ja aivorungon vaikuttaviin soluihin. Tämän tekevät tietyt virukset, jotka toimivat "lautoina" uudelle geneettiselle materiaalille-niin kutsutut adenoon liittyvät virusvektorit (AAV-vektorit).
Vektorigeenikonstruktit annetaan kerran infuusiona laskimoon verenkiertoon ja jaetaan sitten koko kehoon. Koska pienten lasten veri-aivoeste ei ole vielä täysin kehittynyt, nämä vektorit voivat myös päästä selkäydinkudokseen.
Sitomalla nämä vektorit ensisijaisesti motoristen neuronien erityisiin pintarakenteisiin, ne ottavat ensisijaisesti geneettisen materiaalin voidakseen sitten tuottaa SMN -proteiinin itsenäisesti.
Hoito voi parantaa motorisia toimintoja ja johtaa kestävään kehitykseen (esim. Istuminen, ryömiminen ja kävely ilman tukea).Hoidon aikana maksan arvot voivat joskus nousta merkittävästi, mutta verihiutaleiden määrä voi laskea. Kuume ja oksentelu ovat myös yleisiä. Sivuvaikutusten vähentämiseksi potilaille annetaan kortikosteroideja ("kortisoni") muutaman viikon ajan.
Ikää vastaava motorinen kehitys on yleensä mahdollista vain, jos geenihoito on aloitettu oireettomasti. Hoito tapahtuu erikoistuneissa neuromuskulaarisissa hoitokeskuksissa.
fysioterapia
Fysioterapia on edelleen tärkeä tukipilari SMA: n hoidossa, eikä kaikkia SMA -muotoja voida hoitaa uusilla hoitomenetelmillä. Säännöllinen liikuntahoito on suunniteltu ylläpitämään fyysisiä kykyjä ja hidastamaan lihasten hajoamista.
Fysioterapeutti siirtää passiivisesti kehon osia, jotka ovat jo halvaantuneet. Aktiiviset liikesarjat puolestaan on koulutettu tukemaan lihasten liikkuvuutta ja voimaa. Hieronta tai lämpö- ja kylmähoidot voivat myös auttaa. Ne myös rentouttavat ja tietyissä olosuhteissa hidastavat rappeutumista.
Puheterapia
Joissakin tapauksissa SMA vaikuttaa puhuviin ja nieleviin lihaksiin. Sitten puheterapiaharjoitus auttaa. Se kannustaa lapsia oppimaan puhumaan. Jopa vanhemmilla potilailla tämä voi yleensä hidastaa puheen heikkenemistä. Puheterapeutit kouluttavat myös oikean nielemisen.
Sekä fysioterapeutit että puheterapeutit tukevat kohdennettuun hengityshoitoon sairastuneita.
Kipua lievittävä hoito
Kipuhoidolla on tärkeä rooli etenkin taudin edistyneemmissä vaiheissa. Lääkärit käyttävät kipulääkkeitä vähentääkseen kärsivien kärsimystä.
leikkaus
Koska selkärangan lihasatrofia voi johtaa selkärangan vakavaan kaarevuuteen (skolioosi), lääkärit harkitsevat joskus leikkausta. Näin ne jäykistävät erityisesti selkärankaa.
Tämä antaa kärsiville (tietyn) ylimääräisen vartalon vakauden, mikä mahdollistaa pystysuoramman asennon ja suojaa myös luita ja niveliä. Selkäleikkaus voi auttaa myös eteneviä hengitysvaikeuksia vastaan.
Psykoterapeuttinen hoito
Neuromuskulaariset sairaudet, kuten selkärangan lihasatrofia, aiheuttavat suurta psykologista stressiä. Potilaat ja sukulaiset käsittelevät diagnoosin psykoterapian johtamissa yksilö- ja ryhmäistunnoissa ja kehittävät strategioita taudin parantamiseksi.
Myös itsepalveluryhmät ja potilaiden edustajat tarjoavat tärkeää tukea. He ilmoittavat, neuvovat ja tukevat sairastuneita ja heidän sukulaisiaan selviytymään SMA -taudin haasteista.
Mahdollisuudet toipua selkärangan lihasten atrofioista
Jos selkärangan lihasatrofiaa esiintyy, ennuste riippuu ensisijaisesti muodosta. Mitä myöhemmin oireet ilmaantuvat, sitä parempi on kulku. Lisäksi mitä aikaisemmin lääkärit diagnosoivat selkärangan lihasatrofian, sitä nopeammin he voivat aloittaa sopivat hoitotoimenpiteet, jopa ennen kuin motoriset neuronit ovat vaurioituneet peruuttamattomasti.
Uusilla hoitovaihtoehdoilla silmukointimodulaattoreiden ja geenikorvaushoidon avulla on suuri potentiaali proksimaalisen SMA: n hoidossa - varsinkin kun hoito aloitetaan (hyvin) aikaisin. Luotettavan pitkän aikavälin ennusteen tiedot ovat kuitenkin vielä kesken. Vain lisätutkimukset ja tiiviit huumeiden turvallisuushavainnot voivat antaa lisävarmuutta seuraavien (kuukausien ja) vuosien aikana. Uusilla lääkkeillä taudin pitkäaikainen hallinta tai jopa parannus on ainakin mahdollista.
SMA -tyyppi 1 on yleensä vakava sairaus, ja lapsilla, joilla kehittyy tyypin 1 SMA, elinajanodote on (hoitamaton) hyvin rajallinen. Nopeasti lisääntyvä lihasten heikkous koko kehossa vaikuttaa myös hengitykseen. Seurauksena on akuutti keuhkokuume ja jopa hengitysvajaus. Sairastuneet lapset kuolevat ensimmäisten elinvuosien aikana.
Tyypin 2 SMA: n ennuste on hieman parempi. Elinajanodote vaihtelee taudin vakavuuden mukaan: jotkut kuolevat lapsuudessa, mutta suurin osa heistä saavuttaa nuoren aikuisuuden. Ennemmin tai myöhemmin - haluttaessa - hengitystä on tuettava vakavammissa muodoissa. Sairastuneet pysyvät liikkuvina pyörätuolin avulla.
SMA -tyypin 3 kanssa ennuste on huomattavasti parempi - varsinkin jos ensimmäiset oireet ilmestyvät myöhään. Suorituskyky heikkenee vähitellen useiden vuosien aikana. Vanhuudessa pyörätuoli tai jopa pysyvä hoito voi olla tarpeen. Tyypin 3 selkärangan lihasten surkastuminen tuskin rajoittaa elinajanodotetta.
Aikuisten selkärangan lihasatrofia (tyyppi 4) on jopa hitaampi kuin tyyppi 3. Ihmisillä on yleensä normaali elinajanodote.
Tunnisteet: terveet jalat urheilullinen kunto iho